Хелатные комплексы

Надо ли говорить, что производители витаминных комплексов не заморачиваются с хелатной формой, так как она дороже, и добавляют обычную долю минералов и металлов без процесса хелатирования? С точки зрения закона – все правильно, определенная граммовка (или в данном случае милиграммовка соблюдена) на упаковке написано, что присутствует такой-то процент содержания от дневной нормы, и потребитель, довольный и счастливый, покупает эти витамины совершенно не задумываясь о том, как это усвоится.
А усвоится это по-разному. В зависимости от индивидуальных особенностей организма простая форма усвоится от 4 % до 15 %, а вот хелатная от 70 % до 99 %. То есть — с одной стороны, вы вроде бы сэкономите на обычной форме, а с другой — все это просто унесется в бездонные просторы канализации.
Какие еще аргументы можно привести в пользу хелатной формы?
1. Минералы в хелатной форме не затрачивают дополнительных ресурсов на пищеварение и обработку – они уже готовы к использованию клетками эпителия тонкой кишки, где происходит процесс усвоения. Благодаря этому происходит минимизация отторжений организмом и всяческих аллергий на новые препараты

2. Хелатная форма имеет нормальный уровень кислотности и не влияет на уровень желудочной кислотности, тогда как неорганические минералы ощелачивают кислотную среду желудка после приема, что чревато вздутием живота и кишечника, а значит еще большей потерей процента усвоения витаминов, минералов и микроэлементов.
3. Хелатная форма соединений способна проникать через стенку матки беременных и питать развивающийся плод.

Производители уже давно «почувствовали волну», и, к сожалению, на рынке сейчас довольно много якобы хелатных форм, которые по факту являются просто смесью неорганических солей минералов с аминокислотами. Это физическое смешивание не имеет ничего общего с процессом хелации, и никак не повысит процент усвояемости вещества организмом. Чтобы не нарваться на подделку – можно покупать продукты на проверенной площадке с многоэтапной проверкой и сертификацией. Таковой является проверенным временем и лично автором обзора – Интернет-магазин Iherb.com
1. Хелатный кальций
- Поддерживает здоровое состояние костей, зубов и ногтей
- Регулирует нормальную свертываемость крови и внутриклеточные процессы, секрецию гормонов и нейромедиаторов
- Снижает возбудимость нервной системы, повышает устойчивость к стрессу
- Поддерживает эффективность иммунной системы, воздействуя на Т-лимфоциты
- Хелатная форма усваивается на 90-98% в отличие от обычной, где процент равен 5% — 40%
Carlson Labs, Кальций в форме хелата 500 мг, 180 таблеток

Купить
Или Source Naturals, Хелатный кальций, 250 таблеток

Купить
2. Хелатный магний
- Поддерживает здоровье нервной системы
- Расширяет сосуды головного мозга
- Улучшает работу желчного пузыря
- Улучшает внешнее состояние волос и кожи
Bluebonnet Nutrition, Хелатный магний, 120 овощных капсул

Купить
Country Life, Хелатный магния глицинат, 400 мг, 90 таблеток

Купить
3. Хелатное железо
- Необходимо девушкам детородного возраста из-за ежемесячных кровопотерь, а также при ранениях и частых травмах
- Необходимо для обеспечения транспортировки кислорода в ткани и органы
Solgar, Хелат Железа, 100 таблеток

Купить
Bluebonnet Nutrition, Хелатированное железо, 18 мг, 90 капсул в растительной оболочке

Купить
4. Хелатный хром
- Обеспечивает нормальный уровень глюкозы в крови, регулируя выработку инсулина
- Поддерживает здоровье людей, страдающих диабетом
Now Foods, Хром, 500 мкг, 180 вегетарианских капсул

Купить
Source Naturals, Хром, 200 мкг, 250 таблеток

Купить
5. Натуральные мультивитамины с хелатными минералами
Про пользу натуральных мультивитаминов именно с хелатными минералами было сказано в начале обзора. Главная эффект — больший процент усвоения, позволяющий взять комплекс витаминов по более дорогой цене, однако по итогу добиться большей пользы для своего организма.
Solgar, Улучшенный кальциевый комплекс с витаминами D3, К2, цинком и бором, 120 таблеток

Купить
Solgar, Formula V, VM-75, Мультивитамины с хелатными минералами, 90 таблеток

Купить
6. Хелатный цинк
- Требуется для функционирования более 300 ферментов
- Участвует в биосинтезе нуклеиновых кислот и половых гормонов
- Обеспечивает нормальное функционирование головного мозга, повышает память и работоспособность
- Участвует в поддержании здоровья волос, ногтей и кожи
- Обладает обеззараживающими и бактерицидными свойствами, помогает бороться с инфекциями в органах и тканях.
Natural Factors, Хелатный цинк, 25 мг, 90 таблеток

Купить
Источник: xage.ru
На рынке присутствуют разнообразные формы комплексных соединений металлов, используемых в кормлении животных. Все эти разнообразные формы называют «органическими микроэлементами», поскольку входящие в их состав микроэлементы образуют комплексы, или другие типы химических соединений, с органическими молекулами.
Химические процессы комплексообразования, или образования хелатов, понимаются по-разному различными специалистами отрасли кормопроизводства, что приводит к возникновению путаницы в терминах и интерпретации свойств продуктов. Часто встречаются такие термины, как «комплекс металла и аминокислот», «хелат металла и аминокислот», «комплекс металла с полисахаридом», «протеинат металла», однако официальные определения этих терминов расплывчаты и не проясняют ситуацию. В качестве примера в Таблице 1 приведены различные определения органических микроэлементов, используемых в сельском хозяйстве, в формулировках Ассоциации американских контролёров качества кормов (AAFCO, 1998).
Таблица 1. Органические комплексы минералов – определения терминов в формулировках AAFCO.
|
Комплекс металла и аминокислоты – продукт, образующийся при формировании комплекса между растворимой солью металла и аминокислотой. |
|
Хелат металла и аминокислоты — продукт, образующийся в результате реакции иона металла из растворимой соли металла с аминокислотами при молярном соотношении, составляющем один моль металла к одному – трём (предпочтительно, двум) молям аминокислот, с образованием ковалентно-координационных связей. Средняя молекулярная масса гидролизованных аминокислот должна составлять примерно 150, а молекулярная масса образовавшегося хелата не должна превышать 800. |
|
Комплекс металла с полисахаридом — продукт, образующийся при формировании комплекса между растворимой солью и растворённым полисахаридом. |
|
Протеинат металла — продукт, образующийся при образовании хелатов между растворимой солью и аминокислотами и/или частично гидролизованным белком. |
Чтобы разобраться в запутанных определениях, характеризующих химические и физические свойства микроэлементов, прежде всего, необходимо выявить отличия между терминами «комплекс» и «хелат».
Комплексы или хелаты
Термин «комплекс» может использоваться при описании соединений, образующихся при взаимодействии иона металла с молекулой или ионом (лигандом), которые обладают свободной парой электронов. Такие ионы металлов связываются с лигандом посредством атомов-доноров, например, кислорода, азота или серы. Лиганды, обладающие только одним атомом-донором, называются монодентатными, а лиганды, обладающие двумя и более атомами-донорами, называеются би-, три- или тетрадентатными, также их иногда называют полидентатными.
Когда такие лиганды связываются с ионом металла посредством двух и более атомов-доноров, образуется комплекс, состоящий из одного или более гетероцикличных колец, в состав которых входит атом металла. Такие комплексы называются «хелаты» (от греческого «chele» — клешня краба).
Аминокислоты являются бидентатными лигандами, образующими связи с ионами металла посредством кислорода карбоксильной группы и азота аминогруппы.
Этилендиаминтетрауксусная кислота (ЭДТА) является примером гексадентатного лиганда, который содержит шесть атомов-доноров. ЭДТА образует очень прочные комплексы с большинством ионов металлов, и не очень подходит для образования хелатов минералов, поскольку биологическая доступность таких комплексов невысока.
Хотя могут образовываться хелаты, содержащие четыре, пять, шесть или семь колец, установлено, что наиболее стабильными являются хелаты, содержащие пять колец.
Также необходимо помнить о том, что хотя хелаты и являются комплексами, не все комплексы являются хелатами. Несмотря на простоту теории, объясняющей образование хелатов, необходимо строгое соблюдение множества условий для получения стабильного хелата минерала.
Лиганд должен содержать два атома, способных образовывать связи с ионом металла.
Лиганд должен образовывать гетероциклическое кольцо, причём металл должен располагаться «в конце» этого кольца.
Образование хелата металла должно быть пространственно (стерически) возможно. Для достижения стабильности необходимо соблюдать соотношение количества лиганда к минералу.
Истинные хелаты имеют «кольцевую структуру», образованную ковалентно-координационной связью между аминной и карбоксильной группами аминокислоты и ионом металла.
Как правило, хелаты образуются в результате реакции между неорганическими солями минералов, с приготовленной при помощи ферментов смесью аминокислот и небольших пептидов в контролируемых условиях. Такие аминокислотные и пептидные лиганды связываются с ионом металла не в одной точке, а в нескольких, в результате чего атом металла становится частью биологически стабильной кольцевой структуры. Аминокислоты и продукты ферментативного разрушения белков, например, небольшие пептиды, являются идеальными лигандами, поскольку они обладают как минимум двумя функциональными группами (аминной и гидроксильной), необходимыми для образования кольцевой структуры с минералом. Только «переходные элементы», например, медь, железо, марганец и цинк обладают необходимыми физико-химическими характеристиками, позволяющими им образовывать ковалентно-координационные связи с аминокислотами и пептидами с образованием биологически стабильных комплексов.
Аминокислоты и пептиды в качестве лигандов
Существуют различные мнения относительно преимуществ использования аминокислот в сравнении с пептидами при образовании хелатов минералов, ещё больше споров имеется по вопросу биологической доступности таких продуктов. Мы уже рассмотрели общие условия, необходимые для образования биологически стабильных хелатов минералов, однако следует также учитывать и другие факторы, оказывающие влияние на образование хелатов, основными из этих факторов являются:
- Состояние равновесия между количеством ионов металла и количеством лиганда.
- Кинетика реакций замещения между гидратированными ионами металла и имеющимися комплексами.
- Окислительно-восстановительные свойства иона металла и его комплексов.
- Реакции с участием координированных лигандов.
Очевидно, что такой сложный химический феномен не следует чрезмерно упрощать. Однако чтобы прояснить ситуацию касательно преимуществ аминокислот либо пептидов в процессе образования хелатов минералов, мы рассмотрим факторы, влияющие на состояние равновесия и стабильность таких комплексов.
При растворении в воде соли металла, например, сульфата меди (II), с добавлением аминокислоты в качестве бидентатного лиганда, образуется ряд комплексов, каждый из которых обладает собственной константой стабильности, которая зависит от рН раствора. Это показано на Рисунке 1 (реакция сульфата меди (II) с глицином). Из данных, показанных на этом рисунке можно сделать некоторые важные выводы:
- Количество различных содержащих металл соединений при заданных концентрациях металла и аминокислоты зависит от рН раствора.
- Хелаты ионов металла с двойным положительным зарядом не всегда нейтральны.
- Различные ионы металла обладают различными константами стабильности, поэтому количество металла в составе определённых соединений зависит не только от величины рН раствора, но и от константы стабильности комплекса.
Рисунок 1. График изменения содержания меди, включённой в состав различных соединений, при изменении рН в растворе, содержащем медь (II) (0,001М) и глицин (0,002М). Горизонтальная ось: рН. Вертикальная ось: % Cu++

pH
У различных ионов металлов различные константы стабильности. Поэтому, количество металла, входящего в состав конкретного соединения, зависит не только от величины рН раствора, но и от константы стабильности комплекса.
Стабильность содержащего металл комплекса зависит как от свойств металла, так и от свойств лиганда. Увеличение заряда иона, уменьшение размера и увеличение аффинности электронов способствует большей стабильности. На стабильность комплексов влияют также некоторые характеристики лигандов: (1) щёлочность лиганда, (2) количество металло-хелатных колец на единицу лиганда, (3) размер хелатного кольца, (4) пространственные эффекты, (5) резонансные эффекты и (6) атом лиганда. Поскольку комплексные соединения образуются в результате кислотно-основных реакций, как правило, более щелочные лиганды образуют более стабильные комплексы. Также большое значение имеет размер хелатного кольца.
Ещё глубже проанализировав Рисунок 1, можно заметить наличие существенных отличий между относительной стабильностью хелатов металлов, образованных аминокислотами и стабильностью протеинатов металлов. Поскольку протеинат металла является продуктом реакции хелатообразования между растворимой солью и аминокислотами и/или частично гидролизованным белком, можно предположить, что для конкретного иона металла количество графиков, характеризующих образование различных соединений, в состав которых входит металл, при образовании протеината, будет намного больше, чем при образовании хелата этого же металла с аминокислотой. Если считать график, отражающий распределение количества меди между различными соединениями, индикатором относительной стабильности при данной величине рН, и учитывать бесконечное количество комбинаций, возможных в результате взаимодействия как отдельных аминокислот, так и ди-, три- и даже тетрапептидов, то, теоретически, общая стабильность протеината в широком диапазоне рН должна быть намного больше, чем стабильность хелата данного металла с аминокислотой.
Биологическая стабильность
Очевидно, что в реальных условиях рассмотренные дополнительные факторы будут оказывать влияние на стабильность хелата. Однако можно ожидать, что протеинаты металлов будут обладать физико-химическими свойствами, необходимыми для сохранения постоянства характеристик при изменении рН.
Несмотря на наличие некоторой противоречивой информации, образование хелатов металлов – это не такой уж сложный процесс, в основе которого лежат фундаментальные законы химии. Мы можем выделить две формы истинных хелатов минералов, каждая из которых обладает определёнными химическими и биофизическими свойствами. Внимательно изучив факторы, влияющие на образование хелатов минералов, можно выявить различия между продуктами по показателю биологической стабильности и, следовательно, биологической доступности.
Источник: www.dairynews.ru
О роли витаминов и минералов в жизни человека
Организм человека — уникальный и сложнейший «механизм», который в состоянии «работать» на протяжении ста лет и дольше — это не секрет. Целые армии ученых работают над проблемой продления человеческой жизни, и, наверное, в будущем создадут «элексир молодости», но на данный момент вывод ученых таков: ограничения продолжительности жизни зависят от наличия в организме определенного количества важнейших микроэлементов — витаминов и минералов в первую очередь.
Лет тридцать назад эти элементы мы получали с пищей, но в настоящее время из-за катастрофического состояния экологии на нашей планете, дефицит полезных веществ начинают испытывать огромное количество людей. В настоящее время тяжело найти здорового человека, мы страдаем (кто в большей степени, а кто в малой) от той или иной патологии — это из-за нехватки важнейших для нормального функционирования организма, микроэлементов.
Что такое хелаты
Для поддержания здоровья человека и существуют витаминные препараты и различные минеральные комплексы. Но, дело в том, что минералы — неорганическая форма жизни, а наш организм — органическая. И именно по этой причине существует проблема усвоения минералов.
Для решения этой проблемы и существует хелатная форма минералов — соединение минерала с аминокислотой (органики с неорганикой). Эта форма похожа на клешню краба и называется «хелатом» — в переводе с греческого «клешня».
Существуют природные хелаты, известнейший из них — гемоглобин — хелат железа, так же широко известен хлорофилл — хелат магния.
Хелаты: свойства
Эти формы соединений минеральных элементов обладают целым рядом ценных свойств:
— они не токсичны;
— растворяются в воде;
— в широком диапазоне кислотности сохраняют свои свойства;
— хелаты адсорбируются в почве и на листьях;
— устойчивы к губительному воздействию различных микроорганизмов;
— не влияют на уровень желудочной кислоты;
— хелатные формы продолжительное время не разрушаются.
Хелаты — биодоступная форма минералов
Ионы минералов, находясь в соединении с минералами, не требуют дополнительных превращений, чтобы организм их усвоил. Отдельная аминокислота для отдельной клетки — «свой» элемент и именно благодаря этому, хелатные соединения минералов быстро проникают в «свою» клетку.
К примеру, неорганические соли минералов (не хелатная форма) имеют биодоступный уровень около 10%, т.е. 90% их количества, попавших в организм, не усваиваются им, и даже вредят ему.
Хелаты компании Альтера Холдинг
Пожалуй, наиболее эффективные минеральные препараты, которые выпускаются в хелатной форме, это препараты компании Альтера Холдинг. И среди этих препаратов важнейшие для нашего организма:
— хелат железа
— хелат кальция
— кальций магний хелат
— хром хелат
— цинк хелат
Над разработкой этих препаратов трудились ведущие ученые-нутрициологи нашей страны и на сегодняшний день эти препараты не имеют аналогов.
Хотим еще добавить, что при производстве этих препаратов хелатной формы используется передовая технология микрокапсулирования: каждый микроэлемент «помещается» в микрокапсулу, которая «доставляет» этот хелат в определенный отдел организма где происходит его усвоение (важно чтобы хелат усвоился именно в определенном месте, а не где попало).
Хелаты: купить
Купить хелатные комплексы различных минералов у нас двумя способами:
— позвоните нашему менеджеру и закажите препарат;
— сделайте заказ через специальную форму на нашем сайте.
Наша цена на любой препарат на соответствующей странице рядом с его изображением.
Доставка препарата в кратчайшие сроки и без задержек (как по Москве, так и по регионам России, а так же зарубежью), оплата в любой удобной для вас форме.
Хелаты: отзывы
Наталья Евгеньевна М, 58 лет, г. Нальчик
«… 10 лет страдаю остеопорозом, да и сердце побаливает… Мой врач посоветовал мне кальций/магний хелат компании Альтера Холдинг… Пью препарат шесть месяцев, он мне помогает, забыло обо всех болячках…»
Сергей Петрович, 52 года, г. Орел
«… После того, как стал регулярно употреблять цинк хелат, перестал болеть инфекционными заболеваниями, ушли проблемы с простатой…»
Источник: ru-transferfactor.ru
В качестве примера влияния компонентов хелатов на их функцию рассмотрим нуклеиновые кислоты, а также порфириновые, азометиновые и аминокислотные циклические соединения с разными металлами.
Нуклеиновые кислоты
Одними из важнейших хелатов для жизнедеятельности всех живых организмов являются нуклеиновые кислоты (НК). В дезоксирибонуклеиновых (ДНК) и рибонуклеиновых (РНК) кислотах закодирована вся информация, необходимая для развития живого организма; в процессе жизнедеятельности на ее основе происходит синтез всех белков организма из стандартного набора аминокислот.
Основная масса НК сосредоточена в ядрах клеток в составе нуклеопротеинных комплексов, называемых эу— и гетерохроматином. Строение НК очень простое. Скелет гигантских макромолекул составляют полиэфиры фосфорной кислоты и одного из двух пятиуглеродных сахаров — D-рибозы в составе РНК и 2-дезокси-D-рибозы в составе ДНК. Боковые ответвления образованы гетероциклическими основаниями, присоединенными к углеводным компонентам. Их пять: 2 пуриновых — аденин (А) и гуанин (Г) и 3 пиримидиновых — цитозин (Ц) и тимин (Т) в ДНК, и Ц и урацил (У) в РНК (рис. 1).

Рис. 1. Строение НК и оснований
Таким образом, вся молекула НК состоит из чередующихся в различной, но строго определенной последовательности 4 мономерных единиц (нуклеотидов). Они различаются только азотистыми основаниями. Последовательность из 4 нуклеотидов образует структуру первого порядка — первичную структуру НК. Рентгеноструктурные исследования НК показали, что полимерная цепочка молекулы НК любого происхождения закручена в спираль диаметром 2 нм с длиной витка 3,4 нм, так что каждый виток спирали содержит 10 нуклеотидов.
В 1953 г. Д. Уотсон и Ф. Крик, исходя из данных рентгеноструктурного анализа, предложили модель вторичной структуры НК. Для её построения была необходима «главная идея XX века в биологии» — идея матричного размножения биологических макромолекул, автором которой был один из выдающихся биологов того времени Н.К. Кольцов (Шноль, 2010). Без этой идеи невозможно было бы понять структуру молекулы ДНК и предложить её модель. Согласно ей, ДНК образует двуспиральную структуру, стабилизированную водородными связями между азотистыми основаниями, направленными внутрь спирали. При этом водородные связи образуются только между комплементарными парами пиримидин-пурин, то есть Т всегда соединен с А (двумя водородными связями), а Ц или У — с Г (тремя). Эта закономерность объясняется тем, что пара пурин-пурин образовала бы между двумя спиралями слишком длинный мостик, а пиримидин-пиримидин — слишком короткий (рис. 2).

Рис. 2. Спаривание оснований А-Т и Г-Ц
Установлено, что плоскости колец азотистых оснований взаимно параллельны и перпендикулярны оси молекулы, а углеводные кольца расположены в плоскостях, параллельных оси спирали и перпендикулярных азотистым основаниям. Таким образом, вторичная структура ДНК представляет собой жесткое двуспиральное образование. Нити ДНК в ядрах клеток навиты на октамерные комплексы структурных белков гистонов и организованы в структурных единицах хроматина — нуклеосомах. В отличие от гигантских молекул ДНК, более короткие единичные нити молекул РНК становятся двуспиральными благодаря водородным связям, которые местами «завиваются» сами на себя. Затем эти образования сворачиваются в клубок, образуя третичную структуру. Ее конфигурация во многом зависит от окружающей среды, главным образом, от присутствующих ионов металлов.
Как и белки, все НК встречаются в природе только в одной оптической форме. Оптических изомеров НК не обнаружено. Это говорит о существенном значении формы молекулы для ее нормального функционирования в организме. При первых же исследованиях состава НК самого разного происхождения в них были выявлены практически все обычные микроэлементы (Mg, Мп, Са, Zn, Fe, Си и др.), и даже несколько редко обнаруживаемых (Сr, Ni, Sr, Ва, Al, V). В результате очень тщательных экспериментов было выяснено, что эти элементы не являются «примесями». Содержание металлов соответствует постоянным стехиометрическим отношениям к числу мономерных единиц НК. Оно равно для РНК 1:50, а для ДНК 1:150 (Терентьев с соавт., 1968). Были испробованы все обычные методы удаления слабо связанных металлов, например, диализ при разных рН или с подходящими комплексообразующими агентами, и даже переосаждение из растворов, но полностью удалить металлы из состава НК не удалось.
Таким образом, структурно НК представляют собой полидентантные лиганды, где металл имеет «право выбора» своего лиганда между фосфатной, углеводной и азотистой группами. Исследования участков внедрения металлов в НК с помощью методов УФ, ИК-спектроскопии, ЯМР, ЭПР показали, что все металлы можно довольно четко разделить на 2 группы.
Металлы первой группы (Mg, Са, Ва, Sr, Zn, Мп, Ni, Со) связаны электростатическими силами с отрицательно заряженными фосфатными группами. Однако соотношение М:Р отличается от 1:1 и зависит от соотношения А-Т : Г-Ц. Чем больше Г-Ц, тем больше в составе НК связанных металлов. Этот факт легко объяснить тем, что у пары Г-Ц имеются три водородные связи, а у пары А-Т — только две (рис. 3). Поэтому ионы металлов находят в Г-Ц больше участков связывания с основаниями, чем в А-Т. Простое сравнение структур азотистых оснований показывает, что Г напоминает по своему строению 8-оксихинолин — комплексон, обычно используемый в качестве реактива благодаря образованию прочных хелатов с металлами (рис. 3).

Рис. 3. 8-Оксихинолин и гуанин
Поскольку фосфатные группы одной и той же молекулы НК расположены от амино- или окси-групп азотистых оснований слишком далеко, они взаимодействуют с соответствующими группами второй спирали, обеспечивая таким образом стабилизацию двуспиральной структуры ДНК в присутствии ионов металлов.
Итак, металлы первой группы связаны электростатическими силами с отрицательными фосфатными группами, и частично — координационными, через амино- или окси-группы, с азотистыми основаниями (донорно-акцепторной связью, различной силы в зависимости от природы металла). При этом образуются особо прочные пятичленные хелатные узлы (ХУ), соединяющие две спирали.
Вторая группа металлов (Си, Cd, Hg, Pb, Ag, Fe), в соответствии со своими комплексообразующими свойствами, образует прочные хелаты с азотистыми основаниями. Эти металлы обладают повышенным по сравнению с кислородом сродством к азоту. Фосфаты образуют лишь дополнительные связи по остаточным координационным участкам. Каждый из металлов, в зависимости от природы и состояния НК, поступает в определенные наиболее подходящие для него участки молекулы НК, и может выполнять в образовавшейся структуре различные функции.
Обычно основными показателями состояния вторичной структуры ДНК служат величина оптической плотности раствора (ее увеличение коррелирует с процессом деспирализации) и значение температуры плавления (переход нативной ДНК в денатурированную). Стабилизация структуры внешне проявляется уменьшением оптической плотности и увеличением температуры плавления.
Металлы первой группы повышают температуру плавления от 63° до 80°С, причем стабилизирующий эффект прямо пропорционален концентрации металла. Стабилизация двуспиральной структуры ДНК происходит благодаря связыванию металлов с фосфатными группами и уменьшению электростатического отталкивания из-за нейтрализации отрицательных зарядов. При охлаждении все исходные параметры восстанавливаются. Другой возможный тип стабилизации вторичной структуры — дополнительное к водородным связям образование межнуклеотидных мостиков через металл от фосфата к азотистому основанию соседней спирали.
Эффект дестабилизации НК металлами второй группы прямо противоположный. В присутствии Си величина tпл ДНК уменьшается до 42°С, но при охлаждении оптическая плотность существенно не снижается. Вероятно, ионы Си разрушают водородные связи, замещая их при взаимодействии с электроннодонорными группами оснований нуклеотидов. Дело в том, что Н, осуществляющий связь аминогруппы А, пространственно мешает хелатированию, так как лежит в плоскости хелатного узла и затрудняет подход металла для образования пятичленного ХУ. Устранение этого препятствия требует поворота аминогруппы на 90° вокруг оси C-N и, следовательно, разрыва водородной связи между А и комплементарным ему Т. Такое превращение препятствует восстановлению водородных связей при охлаждении, и процесс денатурации становится необратимым. Подобное влияние оказывают также Cd, Hg и Ph. При этом они могут встраиваться непосредственно в водородную связь вместо , Нобразуя прочные хелаты с ковалентной связью (рис. 4).

Рис. 4. Хелатирование ДНК металлами второй группы
Поведение Fe различается в зависимости от валентности. Крупные ионы Fe2+ (радиус 82 пм) увеличивают tпл ДНК, но оптическая плотность раствора при охлаждении не снижается. Объясняется этот эффект начальным связыванием с фосфатом, что приводит к стабилизации по электростатическому механизму, т.е. Fe2+ нейтрализует отрицательные заряды фосфатных групп. Это проявляется повышением tпл. При дальнейшем нагревании и разрыве водородных связей Fe2+ образует хелат с основанием нуклеотида с образованием ковалентных связей, в результате чего его радиус возрастает до 116,5 пм. При охлаждении система водородных связей восстановиться не может. То есть Fe2+ из-за экранирования хелатными узлами тех участков пуринов и пиримидинов, которые обычно спариваются водородными связями, стабилизирует денатурированное состояние ДНК.
В отличие от двухвалентных, меньшие по размеру трехвалентные ионы Fe3+ (радиус 67 пм) внедряются в участках водородных связей, образуя между 2 цепями ДНК хелатные мостики, что стабилизирует двуспиральную структуру. Поэтому при охлаждении ионы Fe3+ эти участки не экранируют, и водородные связи восстанавливаются.
Из этого примера видно, что состояние металла может иметь большое значение для регуляции процессов репликации ДНК в делящейся клетке. Степень окисленности ионов Fe и их противоположная роль в этих процессах зависит от активности ферментов антиоксидантной системы, и поэтому молекулярные механизмы процессов репликации ДНК можно оценить только с учетом содержания в организме металлов и их природы.
Отмеченные особенности связи НК с разными металлами, естественно, проявляются в их функционировании, в частности, в процессах репликации ДНК в фазе G1 и в фазе G2, когда перед вхождением в фазу митоза происходит контроль полноты репликации. Присутствие в клетке в этих фазах металлов второй группы может извратить нормальные процессы репликации, репрессии и активации генов. Более того, под влиянием металлов многие гены необратимо выключаются, то есть теряют способность к транскрипции и никогда впоследствии не экспрессируются. В ряде случаев взаимодействие металлов с ДНК может изменить природу синтезируемых белков, подобно мутации. Наглядно этот механизм можно представить следующим образом (рис. 5).

Рис. 5. Схема изменения репликации ДНК металлами
В норме процесс репликации ДНК состоит из инициации и синтеза цепей ДНК, терминации, взаимодействия с белками хромосом, рекомбинации и репарации ДНК. Расплетание цепи ДНК начинается после того, как ферментная система геликазы связывается со специфической последовательностью нуклеотидов, формируя репликационную вилку. Сразу же за ней по обнажающимся цепям продвигается ДНК-полимераза, которая их реплицирует (схема «А», Гринстейн, 2004).
В присутствии металлов второй группы процесс извращается. На схеме «Б» видно, что хелат М с остатками А и Т не позволяет цепям ДНК расплетаться, и тем самым останавливает репликацию. На схеме «В» показана ветвь спирали ДНК, хелатированная ионом металла; эта ветвь из процесса полимеризации исключается. Цепь ДНК укорачивается на некоторое число нуклеотидов, то есть один или несколько фрагментов Окадзаки ДНК-полимераза пропускает (Леменовский, 1997). В результате два ранее удалённых друг от друга участка ДНК пространственно сближаются. Так как возможность репликации не исчезает, получается ДНК с измененной последовательностью нуклеотидов и в системе передачи структурной информации с помощью РНК синтезируется аномальный белок, как будто произошла мутация (рис. 6).

Рис. 6. Схема репликации ДНК (www.ncbi.nlm.nih.gov/bookshelf/)
Очевидно, что процессы репликации НК зависят не только от фазы клеточного цикла, но и того, в какой ткани они происходят. Высокодифференцированные нейроны или кардиомиоциты у взрослых людей обычно находятся в фазе клеточного цикла G0, когда их деление приостановлено и не возобновляется. В этой фазе клетки экспрессируют белки, используемые не для клеточного деления. Эти белки могут по-разному координироваться имеющимися металлами, от чего их регуляторные функции изменяются и не могут контролироваться рецепторами, локализованными вне или внутри мембран клеток.
Если учесть, что разные металлы влияют на активацию или репрессию генов неодинаково, образующийся в итоге репликации ДНК белок может значительно отличаться от нормального. Подобный механизм может действовать и в активно делящихся клетках. При этом не происходит мутаций или генных нарушений, а лишь под влиянием содержащихся в клетке металлов изменяются процессы декодирования, транскрипции, репликации и трансляции. Состав и соотношение металлов, в свою очередь, зависят от присутствующих в организме эндогенных или экзогенных лигандов, в том числе лекарственных, и от проницаемости мембран для них.
Порфирины
Выше мы уже упоминали значительную роль металлов в широко известных и чрезвычайно биологически важных хелатах — гемоглобине, гемоцианине и хлорофилле. Во всех трех случаях лиганд практически один и тот же — тетрадентантный порфирин, и различаются они заместителями. Однако металлы-комплексообразователи у них разные — соответственно, Fe, Си, Mg — поэтому различается цвет хелатов: красный, голубой, зеленый. Красный гемоглобин и голубой гемоцианин — переносчики O2 и CO2 в крови, соответственно, животных и моллюсков, зеленый хлорофилл — основной источник получения водорода из воды с помощью солнечной энергии в результате биофотолиза и использования протона для синтеза органических соединений. Добавим, что в чёрной крови асцидий O2-переносящий порфирин координирован ещё одним переходным металлом V.
К этой группе хелатов можно отнести и тетрапиррольный корриновый цикл, в котором связь между одной парой пиррольных колец реализована без метиленового мостика, имеющегося у порфиринов. Этот цикл, координированный ионом Со2+, называется «витамином В12» (кобаламин). Кобаламин синтезируется кишечной микрофлорой. Он служит коферментом при конверсии метилмалонил-КоА в сукцинил-КоА, при биосинтезе метионина из гомоцистеина, при восстановлении рибонуклеотидов до дезоксирибонуклеотидов. То есть Со необходим для осуществления важнейших метаболических процессов, связанных с усвоением Fe.
Из ферментов, содержащих витамин В12, наиболее известна метилмалонилмутаза. Ее недостаточность проявляется пернициозной анемией. Развитие недостаточности этого фермента, по-видимому, сопровождается восстановлением Со(II) до Со(I). Последний, будучи сильным нуклеофилом, ковалентно связывает метильную группу и переносит её на другие атомы.
Свойства порфириновых хелатов, содержащих Fe и Си, позволяют им выполнять в метаболизме важнейшую роль переносчиков простых лигандов типа O2 и СO2 или электронов в ферментах дыхательной цепи и в терминальных оксидазах.
Азометины и аминокислоты
К азометинам относятся такие широко известные вещества, как ванилин и другие основания Шиффа. о-Ванилин является промежуточным продуктом реакций дезаминирования, переаминирования и окисления α-аминокислот до α-кетокислот, а также модификации катехоламинов. Он отличается от салицилового альдегида наличием в бензольном кольце альдегидного компонента азометина группы -ОСН3. Эта группа повышает электронную плотность на атоме кислорода фенольной группы, увеличивая степень координации связи металл-лиганд. Растворимость хелатов на основе о-ванилина в неполярных растворителях выше, поэтому они легче проникают через мембраны клеток (рис. 7).

Рис. 7. Салициловая кислота и о-ванилин
Хелаты салициловой оксикислоты (ее эфир с уксусной кислотой — ацетилсалициловая кислота = «аспирин») имеют в метаболизме большое значение, поэтому широко применяются для лечения разнообразных заболеваний. Например, ацетилсалициловая кислота — наиболее широко применяемое во всем мире лекарство. В организме она инактивирует гемсодержащую простагландин-синтазу путем ацилирования остатка серина вблизи активного центра фермента, перекрывая подход к нему арахидоновой кислоты (20:4) и тем самым подавляя синтез простагландина Н2. При этом на некоторое время прерывается действие медиаторов, в данном случае эйкозаноидов, что объясняет болеутоляющее, жаропонижающее и антиревматическое действие препарата (рис. 8).

Рис. 8. Механизм действия аспирина
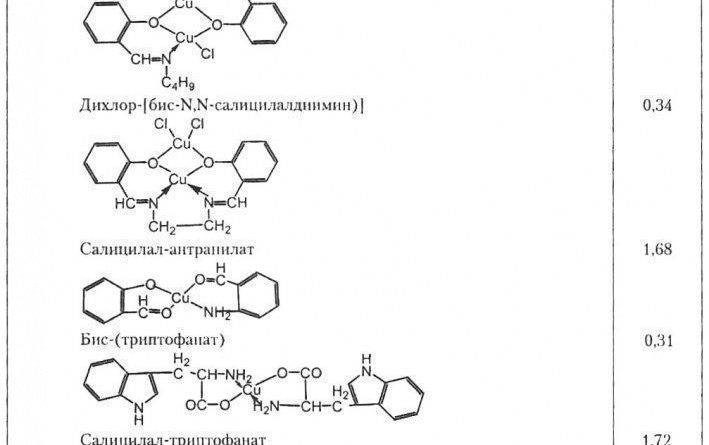
Исследование токсичности азометиновых и аминокислотных хелатов Си, Со, Cr, Zn, Cd, Sn с помощью количественного альготеста (Барашков, Киристаева, 1977) показало, что, в зависимости от очень незначительных изменений в молекуле лигандов, изменяющих конформацию хелатов, токсичность одного и того же металла в расчете на атом меняется на 2-3 порядка. Например, если принять за единицу токсичность тетраэдра (трет-бутилсалицилалимин меди), то токсичность искаженного тстраэдрического металлоцикла (пропилсалицилалимин меди) удваивается, а у квадрипланарного металлоцикла (бутилсалицилалимин меди), наоборот, уменьшается в 20 раз. Можно сказать, что, чем сильнее электроннодонорные группы в молекуле лиганда, тем токсичнее соединение. Напротив, ввод в аминную компоненту азомети-на электроноакцепторной группировки резко снижает токсичность соединения (табл. 1).
Таблица 1. Токсичность металлоциклов меди
Алкилпроизводные хелаты
|
Заместитель |
Строение хелата |
Токсичность |
|
|
R1 |
R2 |
|
Тс |
|
-Н |
-Н |
Плоский |
0,080 |
|
-СН3 -С4Н9 -СН(СН3)2 -С(СН3)3 -СН(СН3)2 -СН3 -С4Н9 |
-Н -Н -Н -Н — С6Н5 -ОСН3 -ОСН3 |
» |
0,076 |
|
» |
0,071 |
||
|
Искаженный тетраэдр |
1,89 |
||
|
» |
1,35 |
||
|
» |
1,10 |
||
|
» |
1,73 |
||
|
» |
2,64 |
||
Общая формула алкилпроизводных хелатов

Арилпроизводные хелаты
|
Заместитель R |
Тс |
|
-Н |
0,50 |
|
-ОСН3 -О2 |
0,32 0,072 |
Общая формула арилпроизводных хелатов

Таким образом, биологическая активность комплексов обусловливается электронным донорно-акцепторным взаимодействием, и поэтому зависит от структуры соединения, природы связи металл-лиганд, природы атома комплексообразователя (металла), констант устойчивости хелатов. Их токсичность и, по-видимому, проницаемость для них биологических мембран усиливаются при введении в орто— и пара-положение к донорным атомам лигандов электроннодонорных группировок.
Выявлен важный факт: биологическая активность кластеров (биметаллических соединений) зависит от структуры соединения в целом, а не от компонентов кластера. Токсичность разнолигандных хелатов, в которых лигандами являются азометин и аминокислота, заметно отличается от токсичности монолигандных хелатов, составляющих кластер (табл. 2).
Таблица 2. Токсичность кластеров и разнолигандных хелатов меди

Это означает, что биологическое действие хелата зависит от проницаемости комплекса в целом. Механизм взаимодействия подобных хелатов и кластеров со структурами мембран пока неясен. По степени влияния на токсичность хелатов с одинаковыми лигандами металлы можно расположить в следующем порядке: в ряду бис-(диокса)-хелатов — Cd>Cu>Co>Zn>Сr, а в ряду бис-(азатиа)-хелатов — Cd>Cu>Zn>Ag>Pb>Co (Рухадзе, Барашков, 1978; Барашков с соавт., 1979).
Эти особенности комплексных соединений необходимо принимать во внимание и при назначении больным, и при разработке лекарств. Небольшие модификации биологически активных молекул могут значительно повлиять на растворимость, проницаемость, константу устойчивости, и тем самым — на физиологические свойства полученных соединений. Механизмы комплексообразования в водных и неводных растворах неодинаковы, то есть в липофильном слое мембран комплексы с металлами образуются не так, как в гидрофильных участках. От этого могут измениться и активность рецепторов, и дальнейшая судьба комплексов.
Медицинская бионеорганика. Г.К. Барашков
Опубликовал Константин Моканов
Источник: medbe.ru
Что такое хелаты
Что такое и зачем нужны хелаты? Название соединений этого типа происходит от chela – клешня по-латыни. Хелаты – особый тип веществ, внешне и по физико-химическим параметрам подобным химическим соединениям в общепринятом понимании. Но строение хелатов принципиально иное. Хелаты находят широкое применение в самых различных областях – от производства оружия массового поражения до фармацевтики, но мы далее ограничимся их свойствами и особенностями использования в качестве удобрений.
Общие понятия
Пример строения хелата показан на рис. справа. Сильный катион (как правило, металла) как бы проваливается в «лунку» органического соединения (в данном случае этилендиаминтетрауксуной кислоты, EDTA), не образуя с ней настоящей химической связи. Вещества, способные хелатировать («цапать») ионы металлов, называются хелатирующими агентами или хелатообразователями. Далее, краткости ради, будем именовать их просто агентами. В свою очередь, «клешня» не дает иону «выпустить» свой электрический заряд и тем самым в полной мере проявить свои химические свойства. Молекулу-«клешню», облекающую ион в хелате, называют лигандом. Металл также влияет на лиганд, т.к. в процессе хелатообразования своим электрическим полем меняет его пространственную конфигурацию (см. рис. ниже), от чего существенно зависят свойства органических соединений. Лиганд в хелате и свободная молекула того же соединения это в сущности разные вещества, поскольку по свойствам отличаются сильнее пространственных изомеров. В результате хелат хорошо растворимого хелатообразователя и активного металла может оказаться химически весьма инертным и нерастворимым, а по виду совершенно непохожим на то и другое. Именно таким оказался первый синтетический хелат, полученный в 1905 г. Л. А. Чугаевым.
Хелаты для удобрений
EDTA очень часто используется для промышленного приготовления удобрительных хелатов, т.к. прочно держит ион и конечные продукты весьма стабильны. Кроме того, этилендиаминтетрауксусная кислота может хелатировать и некоторые неметаллические микроэлементы питания растений, напр. бор. Чтобы хелат EDTA распался, нужно разрушить лиганд или «выдрать» из «клешни» металл. Так, напр., жидкие хелатированные удобрения практически все делаются на основе EDTA. Однако стойкость препарата может быть и помехой, если питательное вещество нужно отдать быстро и/или сквозь преграду, напр. при внекорневой подкормке, см. далее. Поэтому в агротехнике применяются и хелаты с двумя и более молекулами хелатирующих агентов, образующих лигандную оболочку. Используются для этого агенты, поляризованные молекулы которых имеют С-образную или (-образную конфигурацию, напр. лимонная кислота. Их стойкость на хранении ниже, а в растворе фактически нулевая, его нужно вносить немедленно по приготовлении. Но зато такие хелатообразователи не содержат азота и др. балластных или нежелательных в определенных условиях элементов; в почве, на воздухе и свету они быстро распадаются до углекислого газа и воды.
Схемы строения солевого минерального удобрения и хелатного с оболочкой из нескольких лигандов показаны на рис. ниже:
Солевое удобрение это катион – элемент питания E и некоторый неорганический остаток R. Связаны они сильной химической связью (как правило ионной), т.е. валентные электроны E и R образуют общую оболочку. Слабые хелатообразователи ChA берут металл уже не в «клешню», а в кольцо, «дыру» в лигандовой оболочке L. Вся «конструкция» держится уже фактически кулоновскими силами электрического притяжения, в то время как в «клешнях» сильных хелатирующих агентов ионы удерживаются силами, примерно равными таковым координационных химических связей; существенную роль в этом играют квантовые эффекты.
Сравнение сил
Хелатные соединения в целом менее стойки, чем обусловленные «нормальными» химическими связями – они распадаются под влиянием различных внешних факторов: в химически активной среде, под воздействием тепла, света и даже просто на хранении. Поэтому естественных хелатов, напр., в виде горных пород, нет. Но скорость распада хелатов с сильными агентами на порядок-два ниже, чем со слабыми. Это уже качественное различие. Однако в том другом случае «захваченный» ион начинает действовать с задержкой относительно времени внесения удобрения. Именно это обстоятельство важно для агротехники. Поведение вернувшихся к исходной конфигурации молекул агента может быть различным, что также имеет значение.
Поведение в почве
Удобрения на хелатной основе применяются в основном поливом под корень и для подкормок по листьям; реже – в форме водорастворимых гранул или микрокапсул. Плодородная почва – среда влажная, слабокислая или слабощелочная; нейтральные почвы с pH=(6,5-7,5) встречаются как исключение. Вследствие общих свойств хелатов (см. выше) поведение в ней хелатных удобрений существенно отличается от такового солевых.
Солевое удобрение во влажной среде (слева на рис.) немедленно диссоциирует на ионы питательного элемента и остатка. Последний также может содержать питательные элементы или микроэлементы, напр., в калиевой селитре, суперфосфате, калимагнезии, сульфате магния и др. Поскольку ионы весьма подвижны, часть элементов питания неизбежно теряется. Диссоциация это просто-напросто залповый выброс. Концентрация ионов поначалу оказывается слишком высокой, что и понуждает их «разбредаться» как можно скорее. Оказывается возможной ситуация, когда растения недокормлены, а почва вне их объемов питания перенасыщена удобрением, что никак не идет на пользу экологии. Если дозировать внесение по максимуму, то вероятны и химические ожоги корней, и накопление посторонних веществ в плодах (чаще всего – нитратов).
Примечание: в 70-х годах прошлого века Франция и ряд других европейских стран еле пережили «фосфатную катастрофу». Смыв остатков фосфатов с полей вызвал бурное цветение водоемов. Рыба передохла и завонялась, водные биоценозы погибли. Электростанции и предприятия останавливались, водоснабжение и канализация работали с перебоями оттого, что микроводорослями забивались водозаборные и очистные устройства.
Хелатные соединения в почве не диссоциируют, а распадаются на компоненты (справа на рис. выше) прежде всего под влиянием кислотности среды. Распад хелатов идет постепенно, т.к. кислотность почвы обусловлена гуминовыми веществами (ГВ). Расходуются на него почвенные кислоты, в первую очередь фульвовые. Кислотность падает, распад хелатов замедляется, но интенсифицируются процессы образования ГВ. Это снова провоцирует распад хелатов и т.д. Благодаря такому динамическому равновесию питательный элемент выделяется со скоростью, как бы «приноравливающейся» к текущим условиям. В результате вероятность ожогов корней и перекармливания растений уменьшается многократно.
Затем, катионы элемента питания, «не видя» анионов-партнеров, образуют комплексные соединения с другими почвенными кислотами – малоподвижными гуминовыми. Микроток в плодородном слое направлен к «насосам» – корням. Гуматы концентрируются в корневом коме, а вне объема питания их концентрация падает. Это по законам химического равновесия сдвигает почвенные процессы в сторону образования гуминовых кислот. Подвижные фульвовые связываются остатками лигандов и теряют способность быстро и далеко «растаскивать» питательные вещества. В целом же почва лучше сохраняет плодородие и меньше выщелачивается.
EDTA или «лимонка»?
Хелаты на слабых агентах в достаточно тучных и увлажненных почвах распадаются очень быстро. Удобрения на их основе в таких условиях применимы для лечебных (напр. от хлороза) или срочных питательных подкормок, но в качестве текущих сезонных мало эффективны, а вероятность перекармливания растений приближается к таковой минеральными солями.
Удобрения, хелатированные EDTA, на кислых и слабокислых почвах дозируют выделение элементов питания вполне приемлемо. Но один из продуктов их распада – этилен. Этот легкий газ – фитогормон, ускоряющий созревание плодов. Что и может произойти в ущерб их товарным качествам – крупности, сочности, вкусу. В общем, на своем участке начинать применение хелатных удобрений нужно с минимальных рекомендованных инструкцией доз, а далее вносить проверенные.
Примечание: в искусственные субстраты для растений лучше вносить удобрения, хелатированные EDTA. При более свободном, чем в плодородный грунт, доступе воздуха, хелаты этилендиаминтерауксусной кислоты распадаются быстрее, чем в земле, но легких хелатирующих агентов слишком быстро.
Поведение при опрыскивании
Наиболее эффективны удобрения в хелатной форме для внекорневых подкормок как транспортировочные агенты элементов питания, см. рис.:
Ион минерального питательного вещества как правило «отвергается» защитной восковой оболочкой листа, без нее растения «сгорели» бы от обычной пыли. Органический лиганд как бы раздвигает восковую пленку, а затем «захлопывает» ее за собой. Но здесь опять встает вопрос: сильные или слабые хелатообразователи? Многие сильные, и EDTA в том числе, физиологическим циклам в растении мало или совсем не нужны. Растительный организм их быстро нейтрализует, но в результате получаются тот же этилен или свободный азот. Так что внекорневые хелатные подкормки лучше проводить удобрениями на слабых агентах. Ххотя технологически они менее удобны, но, как правило, жизненно необходимы растениям сами по себе. Напр., лимонная кислота, наряду с янтарной – ключевые звенья т. наз. цикла трикарбоновых кислот, чем и объясняется стимулирующее действие удобрений, хелатированных ею.
Примечание: дополнительно о свойствах и особенностях хелатных удобрений см. видео:
Видео: хелатные удобрения — что это такое и для чего нужны?
Когда возможно хелатирование
Химики сначала думали, что хелатировать возможно только металлы. Однако практическая важность хелатов заставляет изыскивать способы «загнать в клешню» и неметаллы. Некоторые, и немалые, успехи в этом налицо, но до технологий хелатирования любых ионов и атомов еще далеко. Поэтому важный фактор, ограничивающий применение хелатных удобрений – сама возможность хелатирования элементов питания растений. Их потребность по сезону вегетации в тех или иных питательных веществах показана на рис.:
Касательно возможности связывания в хелатах питательные элементы распределяются таким образом:
- основные NPK – азот не хелатируется. Лабораторные хелаты фосфора известны, но в агротехнике неприменимы. Калий хелатируется, но такому активному иону нужны очень прочные и стойкие «клешни», что существенно ограничивает применение калийных хелатов на удобрение;
- мезоэлементы – магний и кальций хелатируются EDTA. Соотв. хелаты имеются в продаже как отдельные препараты и применяются по потребности как дополнительные подкормки в случае противопоказаний к основным или микроэлементам;
- микроэлементы – EDTA хелатируются все. В последнее время в продаже появились и хелаты бора как отдельный препарат. Такие важные для лечебных и внеплановых подкормок элементы, как железо и медь, хелатируются слабыми агентами (лимонной кислотой) в кустарных условиях, см. видеоруководство:
Видео: приготовление халатов самостоятельно из железного и медного купороса
Примечание: бор и некоторые другие микроэлементы малоподвижны во внешних средах, но могут вызывать химические ожоги листьев. Дать бора по листьям сразу по потребности растения, он его обожжет. Внести под корень – практически весь потеряется, или корни сожжет, если передозирован. Внесение в хелатной форме решает проблему – в почве хелат выделит его постепенно, а на листе «протащит» сквозь кутикулу без вреда для растения.
Применение хелатных удобрений
И, наконец, один их главных факторов, определяющих применимость хелатных удобрений – их иная, чем у исходных компонент, химическая активность. Среди элементов питания растений известны пары антагонистов, т.е. при совместном внесении мешающих растениям усваивать оба. Классические примеры – фосфор и калий, калий и кальций. Хелатирование одного их антагонистов устраняет проблему – пока хелат «соберется» выделять свой элемент, растение достаточно «наестся» его антагониста. Исходя из всех описанных выше свойств хелатов, удобрения на их основе применимы в таких случаях:
- Комплексные хелатные удобрения – основные NPK даются солями, а мезо- и микроэлементы хелатами. Это устраняет антагонизм элементов и сокращает трудозатраты на обработку – вместо двух или нескольких внесений требуется всего одно. В больших механизированных агрохозяйствах также существенно экономится топливо и ресурс техники.
- Дражирование (инкрустация) семян удобрениями совместно с протравливанием. В сухой плотной среде хелаты EDTA не активны. Добавка хелатированных удобрений для проростков при протравливании семенного материала позволяет существенно увеличить урожайность сравнительно с применением чистых минеральных соединений, см. напр. табл.:
- Микроудобрения в хелатных формах. Исключается антагонизм микроэлементов и ожоги листьев. При необходимости давать лечебные подкормки (железо, магний и др. от хлорозов) можно давать максимальные дозы. Хелатные микроудобрения для ЛПХ – доминирующий продукт в данном сегменте рынка, см. ролик:
Видео: о микроудобрениях в хелатной форме
- Сезонные подкормки по листьям хелатными микроудобрениями. Стимулируют активизируют растения. Основные подкормки не отменяются, но вносятся в меньших дозах, т.к. лучше усваиваются растениями. Общие расходы на удобрения снижаются, экологическая чистота, потребительские качества и количество урожая увеличиваются. В целом хелатные микроподкормки нужны растениям прим. так же, как витамины нам, см. сюжет:
Видео: о хелатных удобрениях как «витаминах» для растений
Хелаты и органика
Хелатированные удобрения вполне применимы в органическом земледелии или в процессе перехода к нему, т.к. исключают залповый выброс в почву активных агентов, нарушающих сложившийся в ней биоценоз. Исключение – заправка почвы натуральным перепревшим (не гранулированным) навозом, навозные парники, теплицы и теплые грядки. Эти способы использования земли сами по себе обеспечивают в ней должный баланс гуматов и фульватов. Избыток хелатов его нарушит, что может вызвать выщелачивание и защелачивание почвы. Если навозная заправка открытого грунта производилась осенью, хелаты на этой площади применимы с весны; если же заправка было весенняя – на следующий сезон. А вот вносить хелатированное питание растений после птичьего помета можно уже через месяц, поскольку помет птиц не влияет коренным образом на баланс почвенных кислот.
Источник: udobreniya.info