Сообщение на тему минеральные удобрения
Органические удобрения применение. Лучший вид полных удобрений. Важной составной их частью является гумус — вещество, восcтанавливающие структуру почвы, улучшающее её поглотительную способность, воздушный и водяной режим, активизирующее деятельность микрофлоры. Органические удобрения обогащают почвы макро- и микроэлементами, витаминами. Навоз-(смешанный, свиной, овечий, конский, крупного рогатого скота) — основное органическое удобрение. В 20 тоннах навоза содержится: азота — 100 кг, фосфора — 50 кг,калия — 120 кг. Наиболее эффективно использовать навоз в свежем виде осенью (октябрь, ноябрь) под перекопку почвы, перед посадкой деревьев и для удобрения растений в приствольных канавках. Если навоз завезён весной или летом, его следует обязательно укрыть настом земли 15-20 см. Перегной — перепревший навоз, лучший вид органического удобрения для подкормки растений. Птичий помёт — наиболее концентрированный вид органических удобрений.
держит азота 2-3%, фосфора 1.5-2%, калия 1%. Под одно дерево вносят 3-5 кг. вещества. Фекалии — содержат много азота и фосфора, мало калия. Лучше всего вносить осенью (не сбраживая) в приствольные канавки и сразу же урывать слоем земли 10-12 см. Под одно дерево 5-6 кг. Компост — органическое удобрение, получаемое из всевозможных отходов: ботва растений, солома, бумага, листья, старые консервные банки, мелкие ветки, пищевые отбросы, гнилые овощи и картофель, бытовой и мелкий строительный мусор — всё кроме стекла, кирпича, плёнки, падалицы фруктов. Для компостирования отходов в конце участка роют яму размером 0.7-0.8 м, обязательно с деревянной крышкой. Некоторые садоводы-любители часто компостируют отходы следующим образом: в междурядьях сада или винограда роют канаву глубиной 30 см., на ширину лопаты укладывают в неё собранные за день отходы и тут же засыпают землёй, продолжая удлинять канаву. Минеральные удобрения. Особенностью минерального удобрения растений является повышенная их потребность в азоте и пониженная в фосфоре (4:1); вынос калия также велик, но его много содержится в глине, недостаток ощущается в песчаной почве. Обозначения основных элементов и соединений: азотные -N, фосфорные — P2O5, калийные — K2O, полные или комплексные минеральные удобрения NPK, к макроэлементам также относятся кальций, магний, железо и сера, к микроэлементам — цинк, молибден, марганец, бор, медь.
Источник: znanija.com
Федеральное агентство по образованию
Тверской государственный технический университет
Кафедра «Технологии полимерных материалов»
Реферат
Производство минеральных удобрений
Выполнила: Томилина О.С.
ФАС, группа БТ-0709
Проверил: Комаров А. М.
Тверь 2010
Минеральными удобрениями называют соли, содержащие элементы, необходимые для питания растений и вносимые в почву для получения высоких и устойчивых урожаев. Минеральные удобрения являются одним из важнейших видов продукции химической промышленности. Рост численности населения выдвигает перед всеми странами мира одну и ту же проблему – умелое управление способностью природы воспроизводить жизненные ресурсы и прежде всего продовольственные. Задача расширенного воспроизводства продуктов питания уже давно решается применением в сельском хозяйстве минеральных удобрений. Научными прогнозами и перспективными планами предусматривается дальнейшее увеличение мирового выпуска минеральных и органоминеральных удобрений, удобрений с регулируемым сроком действия.
Производство минеральных удобрений — одна из важнейших подотраслей химической промышленности, его объем во всем мире составляет более 100млн. т в год. В наибольших количествах вырабатывают и потребляют соединения натрия, фосфора, калия, азота, алюминия, железа, меди, серы, хлора, фтора, хрома, бария и др.
Классификация минеральных удобрений
Минеральные удобрения классифицируют по трем главным признакам: агрохимическому назначению, составу и свойствам.
1. По агрохимическому назначению удобрения делят на прямые, являющиеся источником питательных элементов для растений, и косвенные, служащие для мобилизации питательных веществ почвы улучшением ее физических, химических и биологических свойств. К косвенным удобрениям принадлежат, например, известковые удобрения, применяемые для нейтрализации кислых почв.
Прямые минеральные удобрения могут содержать один или несколько разных питательных элементов.
2. По количеству питательных элементов удобрения подразделяют на простые (одинарные) и комплексные.
В простые удобрения входит только один из трех главных питательных элементов. Соответственно простые удобрения делят на азотные, фосфорные и калийные.
Комплексные удобрения содержат два или три главных питательных элемента. По числу главных питательных элементов комплексные удобрения называют двойными (например, типа NP или РК) или тройными (NPK); последние также называют полными. Удобрения, содержащие значительные количества питательных элементов и мало балластных веществ, называют концентрированными
Комплексные удобрения, кроме того, разделяют на смешанные и сложные. Смешанными называют механические смеси удобрений, состоящие из разнородных частиц, получаемые простым тукосмешением. Если же удобрение, содержащее несколько питательных элементов, получается в результате химической реакции в заводской аппаратуре. Оно называется сложным.
Удобрения, предназначенные для питания растений элементами, стимулирующими рост растений и требующимися в весьма малых количествах, называются микроудобрениями, а содержащиеся в них питательные элементы – микроэлементами. Такие удобрения вносят в почву в очень небольших количествах. К ним относятся соли, содержащие бор, марганец, медь, цинк и другие элементы.
3. По агрегатному состоянию удобрения подразделяют на твердые и жидкие (аммиак, водные растворы и суспензии).
Большое значение имеют физические свойства удобрений. Водорастворимые удобрительные соли должны быть сыпучими, легко рассеиваться, не быть сильно гигроскопичными, не слеживаться при хранении; должны обладать такими, чтобы сохраняться на почве в течение некоторого времени, не слишком быстро вымываться дождевой водой и сдуваться ветром. Этим требованиям в наибольшей мере обладают крупнокристаллические и гранулированные удобрения. Гранулированные удобрения можно вносить не поля механизированными методами с использованием туковых машин и сеялок в количествах, строго соответствующих агрохимическим требованиям.
Фосфорные удобрения
Фосфорные удобрения в зависимости от их состава в различной степени растворимы в почвенных растворах и, следовательно, неодинаково усваиваются растениями. По степени растворимости фосфорные удобрения разделяют на водорастворимые, усвояемые растениями, и нерастворимые фосфаты. К водорастворимым относятся простой и двойной суперфосфаты. К усвояемым, т.е. растворимым в почвенных кислотах, относятся преципитат, термофосфат, плавленые фосфаты и томас-шлак. Нерастворимые удобрения содержат трудноусваемые соли фосфата, растворимые только в сильных минеральных кислотах. К ним фосфоритная мука, апатиты, костяная мука.
Сырьем для производства элементарного фосфата, фосфорных удобрений и других соединений фосфора служат природные фосфаты: апатиты и фосфориты. В этих рудах фосфор находится в нерастворимой форме, главным образом в виде фторапатита Ca5F(PO4)3 или гидроксилапатита Ca5OH(PO4)3. Для получения легкоусваиваемых фосфорных удобрений, применяемых в любых почвах, требуется перевести нерастворимые фосфорные соли природных фосфатов в водорастворимые или легкоусваемые соли. В этом и состоит основная задача технологии фосфорных удобрений.
Растворимость фосфорнокислых солей повышается по мере увеличения их кислотности. Средняя соль Са3(РО4)2 растворима лишь в минеральных кислотах, СаНО4 растворима в почвенных кислотах, а наиболее кислая соль СаН2РО4)2 растворима в воде. В производстве фосфорных удобрений стремятся получить возможно большую часть фосфора в виде монокальцийфосфата Са(Н2РО4)2. Перевод нерастворимых природных солей в растворимые осуществляется разложением их кислотами, щелочами,нагреванием (термическая возгонка фосфора). Одновременно с получением растворимых солей стремятся получить фосфорные удобрения с возможно большей концентрацией фосфора.
Производство суперфосфата
Химическая промышленность выпускает простой и двойной суперфосфаты. Простой суперфосфат – самое распространенное фосфорное удобрение. Он представляет собой порошок (или гранулы) серого цвета, содержащий в основном монофосфат кальция Са(Н2РО4)2*Н2О и сульфат кальция СаSO4*0,5Н2О. В состав суперфосфата входят примеси: фосфаты железа и алюминия, кремнезем, а также фосфорная кислота. Сущность производства суперфосфата состоит в разложении природных фосфатов серной кислотой. Процесс получения суперфосфата при взаимодействии серной кислоты с кальцийфторапатитом является многофазным гетерогенным процессом, протекающим в основном в диффузионной области. Этот процесс можно условно разбить на два этапа. Первый этап – это диффузия серной кислоты к частицам апатита, сопровождаемая быстрой химической реакцией на поверхности частиц, которая идет до полного израсходования кислоты, и кристаллизация сульфата кальция:
Ca5F(PO4)3 + 5H2SO4+2,5H2O=5(CaSO4*0,5H2O)+H3PO4+HF+Q (а)
Второй этап – диффузия образовавшейся фосфорной кислоты в порах неразложившихся частиц апатита, сопровождаемая реакцией
Ca5F(PO4)3+7H3PO4+5H2O=5Ca(H3PO4)2*H2O+HF+Q (б)
Образующийся монокальцийфосфат находится сначала в растворе, при перенасыщении которого начинает кристаллизоваться. Реакция (а) начинается сразу же после смещения и заканчивается в реакционной суперфосфатной камере в течении 20-40 мин в период схватывания и затвердения суперфосфатной массы, которые происходят за счет сравнительно быстрой кристаллизации малорастворимого сульфата кальция и перекристаллизации полугидрата в ангидрит по уравнению реакции
2CaSO4*0,5H2O=2CaSO4+H2O
Последующая стадия процесса – созревание суперфосфата, т.е. образование и кристаллизация монокальцийфосфата, происходит медленно и заканчивается лишь на складе (дозревание) при вылеживание суперфосфата в течение 6-25сут. Малая скорость этой стадии объясняется замедленной диффузией фосфорной кислоты через образовавшуюся корку монокальцийфосфата, покрывающую зерна апатита, и крайне медленной кристаллизацией новой твердой фазы Са(Н2РО4)2*Н2О.
Оптимальный режим в реакционной камере определяется не только кинетикой реакций и диффузией кислот, но и структурой образовавшихся кристаллов сульфата кальция, которая влияет на суммарную скорость процесса и качество суперфосфата. Ускорить диффузионные процессы и реакции (а) и (б) можно повышением начальной концентрации серной кислоты до оптимальной температуры.
Наиболее медленным процессом является дозревание. Ускорить дозревание можно охлаждением суперфосфатной массы и испарением из нее воды, что способствует кристаллизации монокальцийфосфата и повышает скорость реакции (б) вследствие увеличения концентрации Н3РО4 в растворе. Для этого на складе перемешивают и распыляют суперфосфат. Содержание Р2О5 в готовом суперфосфате примерно в два раза ниже, чем в исходном сырье, и составляет при переработке апатитов 19-20% Р2О5.
Готовый суперфосфат содержит некоторое количество свободной фосфорной кислоты, увеличивающей его гигроскопичность. Для нейтрализации свободной кислоты суперфосфат смешивают нейтрализующими твердыми добавками или аммонизируют, т.е. обрабатывают газообразным аммиаком. Эти мероприятия улучшают физические свойства суперфосфата – уменьшают влажность, гигроскопичность, слеживаемость, а при аммонизации вводится еще один питательный элемент – азот.
Существуют периодические, полунепрерывные и непрерывные способы производства суперфосфата. В настоящее время большинство действующих заводов осуществлют непрерывный способ производства. Схема непрерывного способа производства суперфосфата приведена на рис. 1
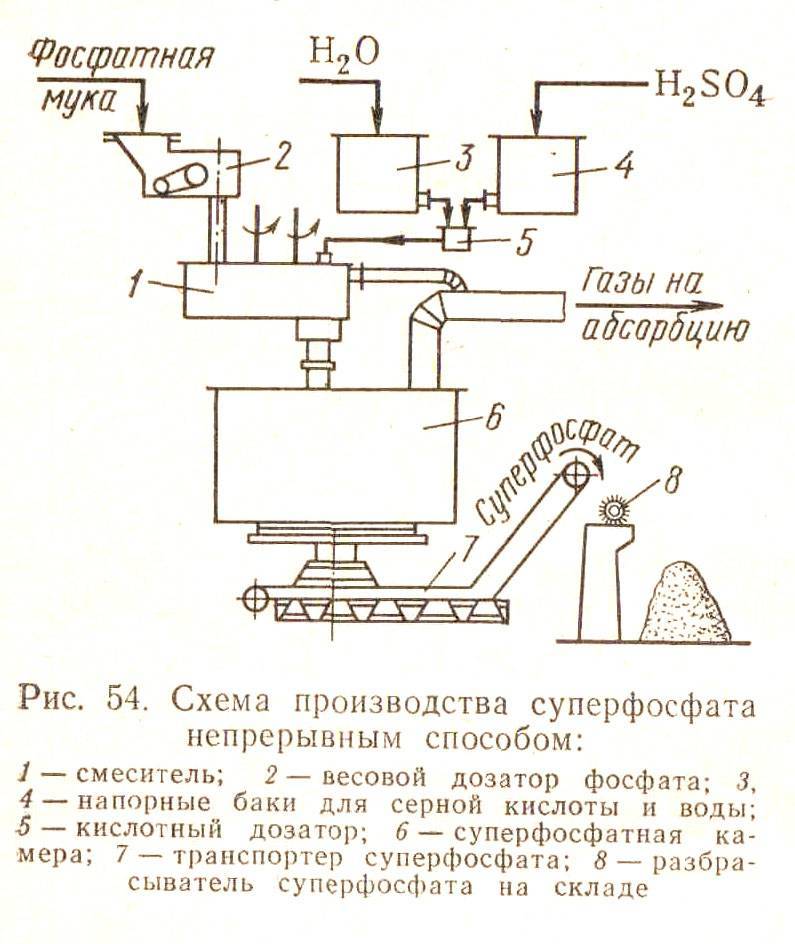
Измельченный апатитовый концентрат (или фосфоритная мука) системой транспортеров, шнеков элеваторов передается со склада на автоматический весовой дозатор, из которого дозируется в смеситель непрерывного действия.
Серная кислота (75%-ная башенная H2SO4) непрерывно разбавляется водой в дозаторе-смесителе до концентрации 68% H2SO4 , контролируемой концентратомером, и подается в смеситель, в котором происходит механическое смешивание фосфатного сырья с серной кислотой. Образующаяся пульпа из смесителя передается в реакционную суперфосфатную камеру непрерывного действия, где происходит образование суперфосфата (схватывание и затвердевание пульпы в начальный период созревания суперфосфатной массы). Из суперфосфатной камеры измельченный суперфосфат подкамерным конвейером передается в отделение дообработки – склад суперфосфата, по которому равномерно распределяется разбрасывателем. Для ускорения дозревания суперфосфата его перемешивают на складе грейферным краном. Для улучшения физических свойств суперфосфата его гранулируют во вращающихся барабанах-грануляторах. В грануляторах порошкообразный суперфосфат увлажняется водой, подаваемой внутрь барабана форсунками, и «закатывается» в гранулы различных размеров, которые затем сушат, рассеивают на фракции и тарируют в бумажные мешки.
Основным аппаратом суперфосфатного производства служит суперфосфатная камера. Питание ее пульпой производится из смесителя, укрепленного непосредственно над крышкой камеры. Для непрерывного питания суперфосфатных камер применяются шнековые смесители и камерные смесители с механическим перемешиванием.
Недостатком простого суперфосфата является сравнительно небольшое содержание питательного элемента – не более 20% Р2О5 из апатитового концентрата и не более 15% Р2О5 из фосфоритов. Более концентрированные фосфорные удобрения можно получить при разложении фосфатной породы фосфорной кислоты.
Азотные удобрения
Большинство азотных удобрений получают синтетически: нейтрализацией кислот щелочами. Исходными материалами для получения азотных удобрений служат серная и азотная кислоты, диоксид углерода, жидкий или газообразный аммиак, гидроксид кальция и т.п. Азот находится в удобрениях или в форме катиона NH4+, т.е. в аммиачной форме, в виде NH2 (амидные), или аниона NO3—, т.е. в нитратной форме; удобрение одновременно может содержать и аммиачный и нитратный азот. Все азотные удобрения водорастворимы и хорошо усваиваются растениями, но легко выносятся вглубь почвы при обильных дождях или орошении. Распространенным азотным удобрением является нитрат аммония или аммиачная селитра.
Производство аммиачной селитры
Аммиачная селитра – безбалластное удобрение, содержащее 35% азота в аммиачной и нитратной форме, благодаря чему она применяется на любых почвах и для любых культур. Однако это удобрения обладает неблагоприятными для его хранения и применения физическими свойствами. Кристаллы и гранулы аммиачной селитры расплываются на воздухе или слеживаются в крупные агрегаты в результате их гигроскопичности и хорошей растворимости в воде. Кроме того при изменении температуры и влажности воздуха во время хранения аммиачной селитры могут происходить полиморфные превращения. Для подавления полиморфных превращений и повышения прочности гранул аммиачной селитры применяют добавки, вводимые в процессе ее изготовления, — фосфаты и сульфаты аммония, борную кислоту, нитрат магния и др. Взрывоопасность аммиачной селитры осложняет ее производство, хранение и транспортировку.
Аммиачную селитру производят на заводах, вырабатывающих синтетический аммиак и азотную кислоту. Производственный процесс складывается из стадий нейтрализации слабой азотной кислоты газообразным аммиаком, упарки полученного раствора и гранулирования аммиачной селитры. Стадия нейтрализации основана на реакции
NH3+HNO3=NH4NO3+148, 6 кДж
Этот хемосорбционный процесс, при котором поглощение газа жидкостью сопровождается быстрой химической реакцией, идет в диффузионной области и сильно экзотермичен. Теплота нейтрализации рационально используется для испарения воды из растворов нитрата аммония. Применяя азотную кислоту высокой концентрации и подогревая исходные реагенты, можно непосредственно получить плав аммиачной селитры (конценрацией выше 95-96% NH4NO3 ) без применения выпаривания.
Наиболее распространены схемы с неполным упариванием раствора аммиачной селитры за счет теплоты нейтрализации (рис. 2).

Основная масса воды упаривается в химическом реакторе –нейтрализаторе ИТН (использование теплоты нейтрализации). Этот реактор – цилиндрический сосуд из нержавеющей стали, внутри которого находится другой цилиндр, куда непосредственно вводится аммиак и азотная кислота. Внутренний цилиндр служит нейтрализационной частью реактора (зона химической реакции), а кольцевое пространство между внутренним цилиндром и корпусом реактора – испарительной частью. Образовавшийся раствор аммиачной селитра поступает из внутреннего цилиндра в испарительную часть реактора, где испарение воды происходит за счет теплообмена между нейтрализационной и испарительной зонами через стенку внутреннего цилиндра. Образовавшийся соковый пар отводится из нейтрализатора ИТН и используется затем как греющий агент.
Сульфатно-фосфатная добавка дозируется в азотную кислоту в виде концентрированных серной и фосфорной кислот, которые нейтрализуются вместе с азотной аммиаком в нейтрализаторе ИТН. При нейтрализации исходной азотной кислоты 58%-ный раствор аммиачной селитры на выходе из ИТН содержит 92-93% NH4NO3; этот раствор направляется в донейтрализатор, в который подается газообразный аммиак с таким расчетом, чтобы раствор содержал избыток аммиака (около 1 г/дм3 своб. NH3), что обеспечивает безопасность дальнейшей работы с плавом NH4NO3. Донейтрализованный раствор концентрируют в комбинированном тарельчатом трубчатом выпарном аппарате с получением плава, содержащего 99,7-99,8% NH4NO3. Для гранулирования высококонцентрированной аммиачной селитры плав погруженными насосами перекачивается наверх грануляционной башни высотой 50-55м. Гранулирование производится разбрызгиванием плава с помощью акустических виброгрануляторов ячеечного типа, обеспечивающих однородный гранулометрический состав продукта. Охлаждение гранул производится воздухом в холодильнике кипящего слоя, состоящем из нескольких последовательных ступеней охлаждения. Охлажденные гранулы опрыскиваются ПАВ в барабане с форсунками и передаются на упаковку.
Ввиду недостатков аммиачной селитры целесообразно изготовление на ее основе сложных и смешанных удобрений. Смешением аммиачной селитры с известняком, сульфатом аммония получают известково-аммиачную селитру, сульфатнитрат аммония и др. Нитрофоску можно получить сплавлением NH4NO3 с солями фосфора и калия.
Производство карбамида
Карбамид (мочевина) среди азотных удобрений занимает второе место по объему производства после аммиачной селитры. Рост производства карбамида обусловлен широкой сферой его применения в сельском хозяйстве. Он обладает большой устойчивостью к выщелачиванию по сравнению с другими азотными удобрениями, т.е. менее подвержен вымыванию из почвы, менее гигроскопичен, может применяться не только как удобрения, но и в качестве добавки к корму крупного рогатого скота. Карбамид, кроме того, широко используется для получения сложных удобрений, удобрений с регулируемым сроком действия, а также для поучения пластмасс, клеев, лаков и покрытий.
Карбамид CO(NH2)2 – белое кристаллическое вещество, содержащее 46.6% азота. Его получение основано на реакции взаимодействия аммиака с диоксидом углерода
2NH3 +CO2=CO(NH2)2+H2O ![]() H=-110,1 кДж (1)
H=-110,1 кДж (1)
Таким образом, сырьем для производства карбамида служат аммиак т диоксид углерода, получаемый в качестве побочного продукта при производстве технологического газа для синтеза аммиака. Поэтому производство карбамида на химических заводах обычно комбинируют с производством аммиака.
Реакция (1) – суммарная; она протекает в две стадии. На первой стадии происходит синтез карбамата:
2NH3+CO2=NH2COONH4 ![]() H=-125,6 кДж (2)
H=-125,6 кДж (2)
газ газ жидкость
На второй стадии протекает эндотермический процесс отщепления воды от молекул карбамата, в результате которого и происходит образование карбамида:
NH2COONH4 = CO(NH2)2+ Н2О ![]() Н=15.5 (3)
Н=15.5 (3)
жидкость жидкость жидкость
Реакция образования карбамата аммония – обратимая экзотермическмя, протекает с уменьшением объема. Для смещения равновесия в сторону продукта ее необходимо проводить при повышенном давлении. Для того, чтобы процесс протекал с достаточно высокой скоростью, необходимы и повешенные температуры. Увеличение давления компенсирует отрицательное влияние высоких температур на смещение равновесия реакции в обратную сторону. На практике синтез карбамида проводят при температурах 150-190 ![]() С и давление 15-20 МПа. В этих условиях реакция протекает с высокой скоростью и до конца.
С и давление 15-20 МПа. В этих условиях реакция протекает с высокой скоростью и до конца.
Разложение карбомата аммония – обратимая эндотермическая реакция, интенсивно протекающая в жидкой фазе. Чтобы в реакторе не происходило кристаллизации твердых продуктов, процесс необходимо вести при температуре ниже 98![]() С (эвтектическая точка для системы CO(NH2)2 — NH2COONH4 ).
С (эвтектическая точка для системы CO(NH2)2 — NH2COONH4 ).
Более высокие температуры смещают равновесие реакции вправо и повышают ее скорость. Максимальная степень превращения карбамата в карбамид достигается при 220![]() С. Для смещения равновесия этой реакции вводят также избыток аммиака, который связывая реакционную воду, удаляет ее из сферы реакции. Однако добиться полного превращения карбамата в карбамид все же не удается. Реакционная смесь по мимо продуктов реакции (карбамида и воды) содержит также карбамат аммония и продукты его разложения – аммиак и СО2.
С. Для смещения равновесия этой реакции вводят также избыток аммиака, который связывая реакционную воду, удаляет ее из сферы реакции. Однако добиться полного превращения карбамата в карбамид все же не удается. Реакционная смесь по мимо продуктов реакции (карбамида и воды) содержит также карбамат аммония и продукты его разложения – аммиак и СО2.
Для полного использования исходного сырья необходимо либо предусмотреть возвращение непрореагировавших аммиака и диоксида углерода, а также углеаммонийных солей (промежуточных продуктов реакции) в колонну синтеза, т.е. создание рецикла, либо отделение карбамида от реакционной смеси и направление оставшихся реагентов на другие производства, например на производство аммиачной селитры, т.е. проведение процесса по открытой схеме.

В крупнотоннажном агрегате синтеза карбамида с жидкостным рециклом и применением стриппинг-процесса (рис. 3) можно выделить узел высокого давления, узел низкого давления и систему грануляции. Водный раствор карбамата аммония и углеаммонийных солей, а также аммиак и диоксид углерода поступают в нижнюю часть колонны синтеза 1 из карбаматного конденсатора высокого давления 4. В колонне синтеза при температуре 170-190![]() С и давлении 13-15 МПа заканчивается образование карбамата и протекает реакция синтеза карбамида. Расход реагентов подбирают таким образом, чтобы в реакторе молярное отношение NH3:CO2 составляло 2,8-2,9. Жидкая реакционная смесь (плав) из колонны синтеза карбамида поступает в отдувочную колонну 5, где стекает по трубам вниз. Противотоком к плаву подают сжатый в компрессоре до давления 13-15МПа диоксид углерода, к которому для образования пассивирующей пленки и уменьшения коррозии оборудования добавлен воздух в количестве, обеспечивающем в смеси концентрацию кислорода 0,5-0,8%. Отдувочная колонна обогревается водяным паром. Парогазовая смесь из колонны 5, содержащая свежий диоксид углерода, поступает в конденсатор высокого давления 4. В него же вводят жидкий аммиак. Он одновременно служит рабочим потоком в инжекторе 3, подающем в конденсатор раствор углеаммонийных солей из скруббера высокого давления 2 и при необходимости часть плава из колонны синтеза. В конденсаторе образуется карбамат. Выделяющуюся при реакции теплоту используют для получения водяного пара.
С и давлении 13-15 МПа заканчивается образование карбамата и протекает реакция синтеза карбамида. Расход реагентов подбирают таким образом, чтобы в реакторе молярное отношение NH3:CO2 составляло 2,8-2,9. Жидкая реакционная смесь (плав) из колонны синтеза карбамида поступает в отдувочную колонну 5, где стекает по трубам вниз. Противотоком к плаву подают сжатый в компрессоре до давления 13-15МПа диоксид углерода, к которому для образования пассивирующей пленки и уменьшения коррозии оборудования добавлен воздух в количестве, обеспечивающем в смеси концентрацию кислорода 0,5-0,8%. Отдувочная колонна обогревается водяным паром. Парогазовая смесь из колонны 5, содержащая свежий диоксид углерода, поступает в конденсатор высокого давления 4. В него же вводят жидкий аммиак. Он одновременно служит рабочим потоком в инжекторе 3, подающем в конденсатор раствор углеаммонийных солей из скруббера высокого давления 2 и при необходимости часть плава из колонны синтеза. В конденсаторе образуется карбамат. Выделяющуюся при реакции теплоту используют для получения водяного пара.
Из верхней части колонны синтеза непрерывно выходят непрореагировавшие газы, поступающие в скруббер высокого давления 2, в котором большая часть их конденсируется вследствие водного охлаждения, образуя раствор карбамата и углеаммонитйных солей.
Водный раствор карбамида, выходящий из отдувочной колонны 5, содержит 4-5% карбамата. Для окончательного его разложения раствор дросселируют до давления 0,3-0,6 МПа и затем направляют в верхнюю часть ректификационной колонны 8.
Жидкая фаза стекает в колонне вниз по насадке противотоком к парогазовой смеси, поднимающейся снизу вверх. Из верхней части колонны выходят NH3,CO2 и водяные пары. Водяные пары конденсируются в конденсаторе низкого давления 7, при этом растворяется основная часть аммиака и диоксида углерода. Полученный раствор направляют в скруббер 2. Окончательная очистка газов, выбрасываемых в атмосферу, проводится абсорбционными методами.
70%-ный раствор карбамида, выходящий из нижней части ректификационной колонны 8, отделяют от парогазовой смеси и направляют после снижения давления до атмосферного сначала на выпарку, а затем на грануляцию. Перед распылением плава в грануляционной башне 12 к нему добавляют кондиционирующие добавки, например мочевиноформальдегидную смолу, чтобы получить неслеживающееся удобрение, не портящееся при хранении.
Охрана окружающей среды при производстве удобрений
При производстве фосфорных удобрений велика опасность загрязнения атмосферы фтористыми газами. Улавливание соединений фтора важно не только с точки зрения охраны окружающей среды, но также и потому, что фтор является ценным сырьем для получения фреонов, фторопластов, фторкаучуков и т.д. Соединения фтора могут попасть в сточные воды на стадиях промывки удобрений, газоочистки. Целесообразно для уменьшения количества таких сточных вод создавать в процессах замкнутые водооборотные циклы. Для очистки сточных вод от фтористых соединений могут быть применены методы ионного обмена, осаждения с гидроксидами железа и алюминия, сорбции на оксиде алюминия и др.
Сточные воды производства азотных удобрений, содержащие аммиачную селитру и карбамид, направляют на биологическую очистку, предварительно смешивая их с другими сточными водами в таких соотношениях, чтобы концентрация карбамида не превышала 700мг/л, а аммиака – 65-70мг/л.
Важной задачей в производстве минеральных удобрений является очистка газов от пыли. Особенно велика возможность загрязнения атмосферы пылью удобрений на стадии грануляции. Поэтому газ, выходящий из грануляционных башен, обязательно подвергается пылеочистке сухими и мокрыми методами.
Список литературы
-
А.М. Кутепов и др.
Общая химическая технология: Учеб. для вузов/А.М. Кутепов,
Т.И. Бондарева, М.Г. Беренгартен.- 3-е изд., перераб. – М.: ИКЦ «Академкнига». 2003. – 528с.
-
И.П. Мухленов, А.Я. Авербух, Д.А Кузнецов, Е.С. Тумаркина,
И.Э. Фурмер.
Общая химическая технология: Учеб. для химико-техн. спец. вузов.
В 2х томах. Т.2. Важнейшие химические производства/ И.П. Мухленов, А.Я. Кузнецов и др.; Под ред. И.П. Мухленова. – 4-е изд., перераб. и доп. – М.: «Высш. шк.», 1984.-263 с., ил.
-
Бесков В. С.
Общая химическая технология: Учебник для вузов. – М.: ИКЦ «Академкнига», 2005. -452с.: ил.
Источник: works.doklad.ru
Органические удобрения применение. Лучший вид полных удобрений. Важной составной их частью является гумус — вещество, восcтанавливающие структуру почвы, улучшающее её поглотительную способность, воздушный и водяной режим, активизирующее деятельность микрофлоры. Органические удобрения обогащают почвы макро — и микроэлементами, витаминами. Навоз — (смешанный, свиной, овечий, конский, крупного рогатого скота) — основное органическое удобрение. В 20 тоннах навоза содержится: азота — 100 кг, фосфора — 50 кг, калия — 120 кг. Наиболее эффективно использовать навоз в свежем виде осенью (октябрь, ноябрь) под перекопку почвы, перед посадкой деревьев и для удобрения растений в приствольных канавках. Если навоз завезён весной или летом, его следует обязательно укрыть настом земли 15-20 см. Перегной — перепревший навоз, лучший вид органического удобрения для подкормки растений. Птичий помёт — наиболее концентрированный вид органических удобрений. Содержит азота 2-3%, фосфора 1.5-2%, калия 1%. Под одно дерево вносят 3-5 кг. вещества. Фекалии — содержат много азота и фосфора, мало калия. Лучше всего вносить осенью (не сбраживая) в приствольные канавки и сразу же урывать слоем земли 10-12 см. Под одно дерево 5-6 кг. Компост — органическое удобрение, получаемое из всевозможных отходов: ботва растений, солома, бумага, листья, старые консервные банки, мелкие ветки, пищевые отбросы, гнилые овощи и картофель, бытовой и мелкий строительный мусор — всё кроме стекла, кирпича, плёнки, падалицы фруктов. Для компостирования отходов в конце участка роют яму размером 0.7-0.8 м, обязательно с деревянной крышкой. Некоторые садоводы-любители часто компостируют отходы следующим образом: в междурядьях сада или винограда роют канаву глубиной 30 см., на ширину лопаты укладывают в неё собранные за день отходы и тут же засыпают землёй, продолжая удлинять канаву. Минеральные удобрения. Особенностью минерального удобрения растений является повышенная их потребность в азоте и пониженная в фосфоре (4:1); вынос калия также велик, но его много содержится в глине, недостаток ощущается в песчаной почве. Обозначения основных элементов и соединений: азотные — N, фосфорные — P2O5, калийные — K2O, полные или комплексные минеральные удобрения NPK, к макроэлементам также относятся кальций, магний, железо и сера, к микроэлементам — цинк, молибден, марганец, бор, медь.
Источник: iotvet.com
 |
Здесь можно найти учебные материалы, которые помогут вам в написании курсовых работ, дипломов, контрольных работ и рефератов. Так же вы мажете самостоятельно повысить уникальность своей работы для прохождения проверки на плагиат всего за несколько минут.
|
|
|
